تفاوت کلیدی - متان در مقابل اتان
متان و اتان کوچکترین اعضای خانواده آلکان هستند. فرمول مولکولی این دو ترکیب آلی به ترتیب CH4 و C2H6 است. تفاوت اصلی بین متان و اتان ساختار شیمیایی آنها است. یک مولکول اتان را می توان به عنوان دو گروه متیل در نظر گرفت که به عنوان دایمر گروه های متیل به هم متصل شده اند. سایر تفاوت های شیمیایی و فیزیکی عمدتاً به دلیل این تفاوت ساختاری ایجاد می شود.
متان چیست؟
متان کوچکترین عضو خانواده آلکانها با فرمول شیمیایی CH4است (چهار اتم هیدروژن به یک اتم کربن پیوند دارند).جزء اصلی گاز طبیعی محسوب می شود. متان گازی بی رنگ، بی بو و بی مزه است. همچنین به عنوان کربن، گاز مرداب، گاز طبیعی، تترا هیدرید کربن و کاربید هیدروژن شناخته می شود. می توان آن را به راحتی مشتعل کرد و بخار آن از هوا سبک تر است.
متان به طور طبیعی در زیر زمین و زیر کف دریا یافت می شود. متان اتمسفر به عنوان گاز گلخانه ای در نظر گرفته می شود. متان با آب موجود در جو به CH3 تجزیه می شود.
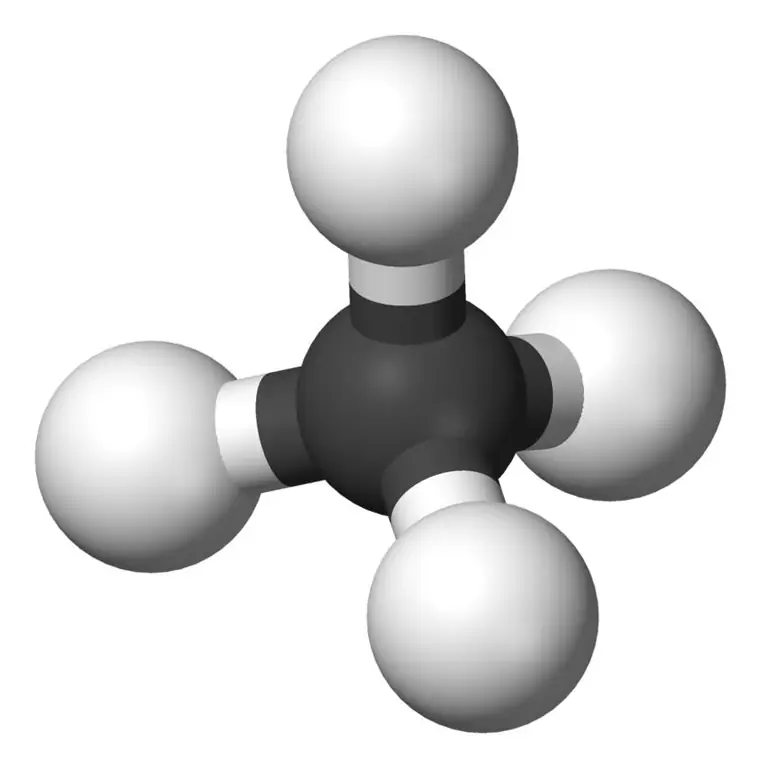
اتان چیست؟
اتان یک ترکیب گازی بی رنگ و بی بو در دما و فشار استاندارد است. فرمول مولکولی و وزن مولکولی آن به ترتیب C2H6 و 30.07 g·mol−1 است. از گاز طبیعی به عنوان یک محصول جانبی از فرآیند پالایش نفت جدا می شود.اتان در تولید اتیلن بسیار مهم است.
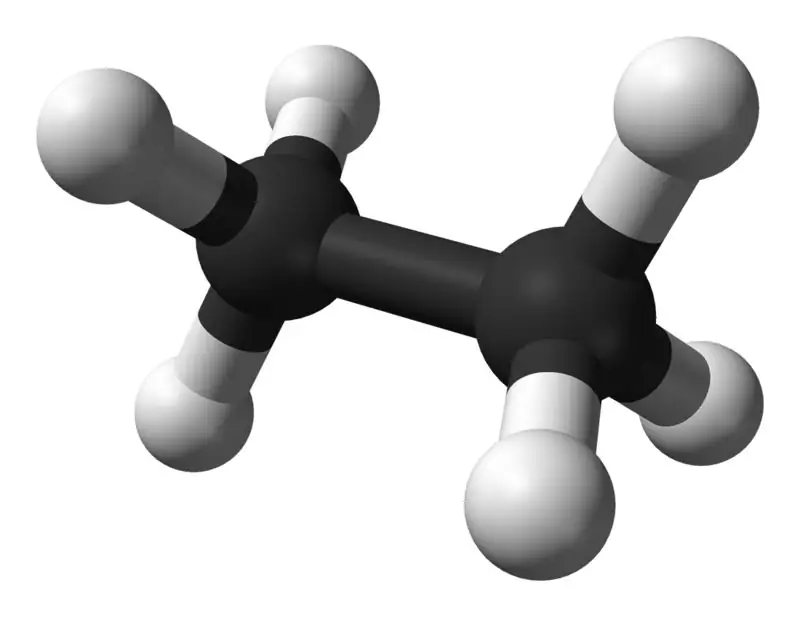
تفاوت بین متان و اتان چیست؟
ویژگی های متان و اتان
ساختار:
متان: فرمول مولکولی متان CH4، است و نمونه ای از یک مولکول چهار وجهی با چهار پیوند C-H معادل (پیوند سیگما) است. زاویه پیوند بین اتم های H-C-H 109.50 است و همه پیوندهای C-H معادل هستند و برابر است با 108.70 pm.
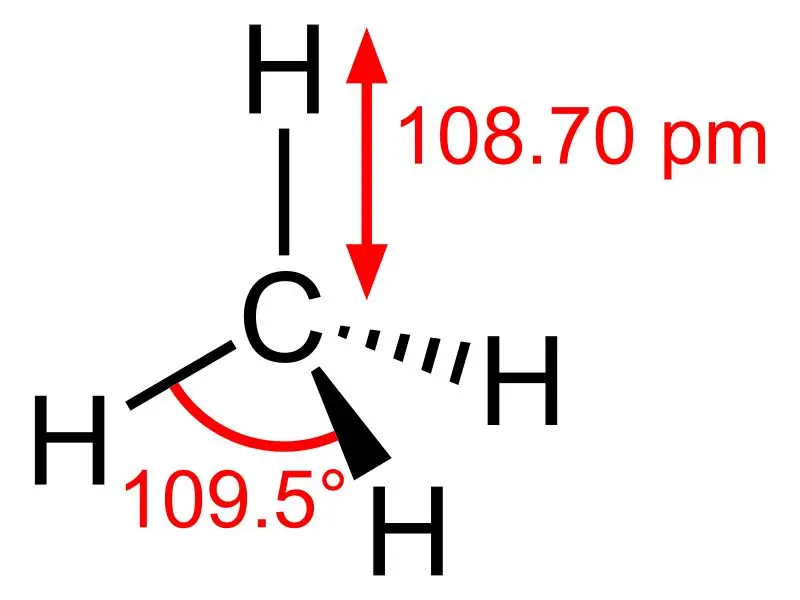
اتان: فرمول مولکولی اتان C2H6،است و یک هیدروکربن اشباع است زیرا حاوی پیوندهای متعدد نیست..
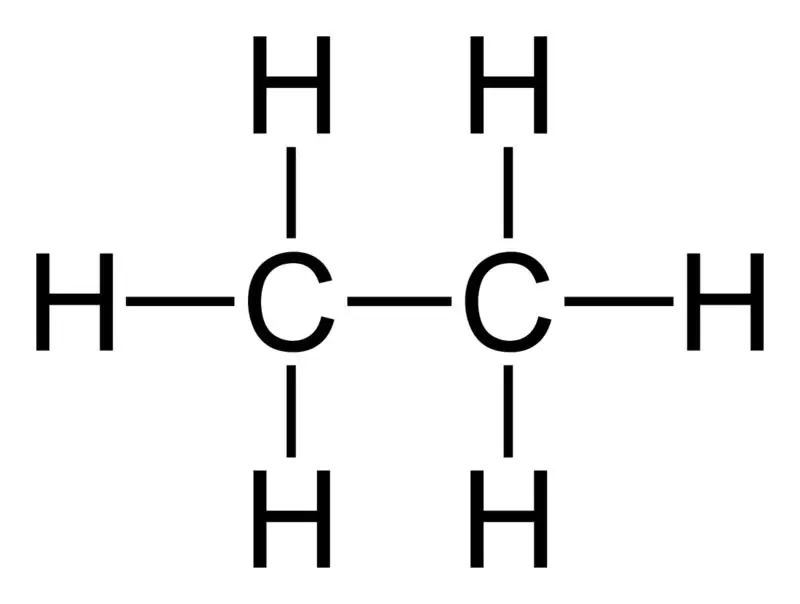
خواص شیمیایی:
متان:
پایداری: متان یک مولکول شیمیایی بسیار پایدار است که با KMnO4، K2Cr واکنش نمی دهد. 2O7، H2SO4 یا HNO 3 در شرایط عادی.
احتراق: در مجاورت هوا یا اکسیژن اضافی، متان با شعله غیر درخشان آبی کم رنگ می سوزد و دی اکسید کربن و آب تولید می کند. این یک واکنش بسیار گرمازا است. بنابراین، به عنوان یک سوخت عالی استفاده می شود. در حضور هوا یا اکسیژن کافی، تا حدی به گاز مونوکسید کربن (CO) می سوزد.
واکنشهای جانشینی: متان واکنشهای جانشینی را با هالوژن نشان میدهد. در این واکنش ها یک یا چند اتم هیدروژن با تعداد مساوی اتم هالوژن جایگزین می شود و به آن هالوژناسیون می گویند.در مجاورت نور خورشید با کلر (Cl) و برم (Br) واکنش می دهد.
واکنش با بخار: وقتی مخلوطی از متان و بخار از طریق نیکل گرم شده (1000 K) که روی سطح آلومینا قرار دارد عبور داده شود، می تواند هیدروژن تولید کند.
پیرولیز: وقتی متان تا حدود 1300 کلوین گرم می شود، به کربن سیاه و هیدروژن تجزیه می شود.
اتان:
واکنش ها: گاز اتان (CH3CH3) با بخار برم در حضور نور واکنش می دهد و برمواتان را تشکیل می دهد (CH 3CH2Br) و هیدروژن بروماید (HBr). این یک واکنش جایگزینی است. یک اتم هیدروژن در اتان با اتم برم جایگزین می شود.
CH3CH3 + Br2 à CH3 CH2Br + HBr
احتراق: احتراق کامل اتان 1559.7 کیلوژول بر مول (51.9 کیلوژول بر گرم) گرما، دی اکسید کربن و آب تولید می کند.
2 C2H6 + 7 O2 → 4 CO 2 + 6 H2O + 3120 کیلوژول
همچنین می تواند بدون اکسیژن اضافی رخ دهد و ترکیبی از کربن آمورف و مونوکسید کربن تولید کند.
2 C2H6 + 3 O2 → 4 C + 6 H 2O + انرژی
2 C2H6 + 5 O2 → 4 CO + 6 H 2O + انرژی
2 C2H6 + 4 O2 → 2 C + 2 CO + 6 H2O + انرژی و غیره.
تعریف:
واکنشهای جانشینی: واکنش جانشینی یک واکنش شیمیایی است که شامل جابجایی یک گروه عاملی در یک ترکیب شیمیایی و جایگزینی آن با یک گروه عاملی دیگر است.
موارد استفاده:
متان: متان در بسیاری از فرآیندهای شیمیایی صنعتی (به عنوان سوخت، گاز طبیعی، گاز طبیعی مایع) استفاده می شود و به عنوان یک سیال در یخچال حمل می شود.
اتان: اتان به عنوان سوخت برای موتورها و به عنوان مبرد برای سیستم هایی با دمای بسیار پایین استفاده می شود. این در سیلندرهای فولادی به عنوان گاز مایع تحت فشار بخار خود حمل می شود.







