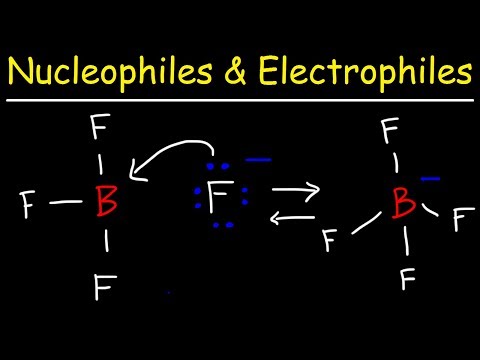
تفاوت اصلی بین نوکلئوفیل و الکتروفیل این است که هسته دوست ماده ای است که به دنبال مرکز مثبت است در حالی که الکتروفیل ها به دنبال مراکز منفی هستند که الکترون های اضافی دارند.
میتوان گونههایی را که در اثر جداسازی بار به وجود میآیند، "الکتروفیل" و "هسته دوست" نامید. در این مقاله دقیقاً نوکلئوفیل یا الکتروفیل چیست. الکتروفیل ها و هسته دوست ها برای شروع واکنش های شیمیایی مهم هستند. علاوه بر این، آنها برای توصیف چگونگی ادامه واکنش ها مهم هستند. در شیمی آلی، میتوانیم مکانیسمهای واکنش را بسته به گونههای اولیه (اعم از الکتروفیل یا هسته دوست) که شروع به حمله به گونههای دیگر میکنند، دستهبندی کنیم.جایگزینی هسته دوست، افزودن هسته دوست، جایگزینی الکتروفیل و افزودن الکتروفیل چهار نوع مکانیسم اصلی توصیف کننده واکنش های آلی هستند.
نوکلئوفیل چیست؟
نوکلئوفیل هر یون منفی یا هر مولکول خنثی است که حداقل یک جفت الکترون مشترک داشته باشد. نوکلئوفیل ماده ای است که بسیار الکترومثبت است، بنابراین دوست دارد با مراکز مثبت تعامل داشته باشد. می تواند با استفاده از جفت الکترون تنها واکنش ها را آغاز کند. به عنوان مثال، هنگامی که یک هسته دوست با یک آلکیل هالید واکنش می دهد، جفت تک هسته دوست به اتم کربنی که حامل هالوژن است حمله می کند. این اتم کربن به دلیل تفاوت بین مقادیر الکترونگاتیوی این کربن و اتم هالوژن دارای بار مثبت جزئی است. پس از اتصال هسته دوست به کربن، هالوژن خارج می شود. ما این نوع واکنش ها را واکنش های جانشینی هسته دوست می نامیم.

شکل 01: یک واکنش افزودنی هسته دوست
نوع دیگری از واکنش وجود دارد که هسته دوست ها می توانند آغاز کنند. ما آن را واکنش حذف هسته دوست می نامیم. هسته دوستی در مورد مکانیسم های واکنش می گوید. بنابراین، این نشانه ای از سرعت واکنش است. به عنوان مثال، اگر هسته دوستی زیاد باشد، واکنش خاصی سریع می شود و اگر هسته دوستی کم باشد، سرعت واکنش کند است. از آنجایی که هسته دوست ها الکترون اهدا می کنند، طبق تعریف لوئیس، آنها باز هستند.
Electrophile چیست؟
الکتروفیل ها معرف هایی هستند که در واکنش های خود به دنبال الکترون های اضافی هستند که به آنها یک لایه ظرفیتی پایدار از الکترون ها بدهد. کربوکاتیون ها الکتروفیل هستند. آنها کمبود الکترون دارند و تنها شش الکترون در لایه ظرفیت خود دارند. به همین دلیل، کربوکاتیون ها می توانند به عنوان اسیدهای لوئیس عمل کنند. آنها یک جفت الکترون را از یک هسته دوست می پذیرند و پوسته ظرفیت را پر می کنند.

شکل 02: یک واکنش افزودنی الکتروفیلیک
الکتروفیل ها ممکن است دارای بار مثبت رسمی، بار مثبت جزئی یا پوسته والانس با هشت ناقص باشند. واکنش های جایگزینی الکتروفیل و افزودن الکتروفیل دو واکنش عمده ای هستند که الکتروفیل ها می توانند شروع کنند. در یک واکنش جایگزینی الکتروفیل، یک الکتروفیل یک اتم یا گروه را در یک ترکیب جابجا می کند. ما می توانیم این حادثه را عمدتاً در ترکیبات معطر مشاهده کنیم. به عنوان مثال، این مکانیسم هایی است که یک گروه نیترو با جابجایی هیدروژن به حلقه بنزن متصل می شود. در واکنش افزودن الکتروفیلیک، یک پیوند پی در یک مولکول شکسته میشود و یک پیوند سیگما جدید بین مولکول و الکتروفیل تشکیل میشود.
تفاوت بین هسته دوست و الکتروفیل چیست؟
یک هسته دوست هر یون منفی یا هر مولکول خنثی است که حداقل یک جفت الکترون مشترک داشته باشد، در حالی که الکتروفیلها معرفهایی هستند که در واکنشهای خود به دنبال الکترونهای اضافی هستند که به آنها لایه ظرفیتی پایداری از الکترونها بدهد. بنابراین، تفاوت اصلی بین نوکلئوفیل و الکتروفیل در این است که هسته دوست ماده ای است که به دنبال یک مرکز مثبت است در حالی که الکتروفیل ها به دنبال مراکز منفی هستند که الکترون های اضافی دارند. علاوه بر این، میتوانیم نوکلئوفیلها را بهعنوان بازهای لوئیس در نظر بگیریم در حالی که الکتروفیلها را بهعنوان اسیدهای لوئیس در نظر بگیریم. از این رو، این تفاوت دیگری بین نوکلئوفیل و الکتروفیل است.
اینفوگرافیک زیر تفاوت بین نوکلئوفیل و الکتروفیل را به عنوان مقایسه ای کنار هم نشان می دهد.

خلاصه - هسته دوست در مقابل الکتروفیل
نوکلئوفیل ها و الکتروفیل ها دو شکل مختلف از گونه های شیمیایی هستند که توانایی شروع واکنش های شیمیایی مختلف را دارند. تفاوت اصلی بین نوکلئوفیل و الکتروفیل در این است که هسته دوست ماده ای است که به دنبال یک مرکز مثبت است در حالی که الکتروفیل ها به دنبال مراکز منفی هستند که الکترون های اضافی دارند.