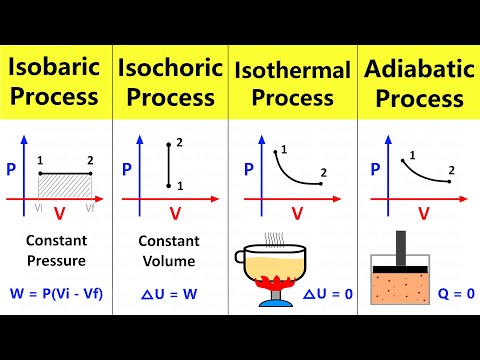
تفاوت اصلی بین فرآیند ایزوباریک و ایزوکوریک در این است که فرآیند ایزوباریک در یک فشار ثابت رخ می دهد در حالی که فرآیند ایزوباریک در یک حجم ثابت رخ می دهد.
فرآیند ترمودینامیکی یک فرآیند شیمیایی یا فیزیکی است که در یک سیستم ترمودینامیکی اتفاق می افتد و سیستم را از حالت اولیه به حالت نهایی تغییر می دهد. انواع مختلفی از فرآیندهای ترمودینامیکی وجود دارد. فرآیندهای ایزوباریک و ایزوکوریک دو فرآیند از این قبیل هستند.
فرایند ایزوباریک چیست؟
فرایند ایزوباریک یک فرآیند شیمیایی است که در یک سیستم ترمودینامیکی تحت فشار ثابت انجام می شود.بنابراین تغییر فشار یا ∆P صفر است. معمولاً سیستم فشار را ثابت نگه میدارد تا حجم سیستم تغییر کند. می تواند انبساط یا انقباض باشد. این تغییر در حجم می تواند تغییرات فشار را که ممکن است در اثر انتقال حرارت بین سیستم و محیط اطراف رخ دهد خنثی کند.

شکل 01: کار انجام شده در یک فرآیند ایزوباریک (ناحیه زرد)
معمولاً، در یک فرآیند ایزوباریک، انرژی داخلی (U) تغییر می کند. بنابراین کار (W) توسط سیستم در حین انتقال حرارت انجام می شود. میتوانیم کار را در فشار ثابت با استفاده از رابطه زیر محاسبه کنیم.
W=P∆V
در اینجا W کار، P فشار و ∆V تغییر حجم است. بنابراین، اگر انتقال حرارت باعث انبساط حجم سیستم شود، سیستم یک کار مثبت انجام می دهد در حالی که اگر انتقال حرارت باعث انقباض حجم سیستم شود، سیستم کار منفی انجام می دهد.
فرآیند ایزوکوریک چیست؟
فرایند ایزوکوریک یک فرآیند شیمیایی است که در یک سیستم ترمودینامیکی تحت حجم ثابتی انجام می شود. بنابراین، تغییری در حجم وجود ندارد; ΔV صفر است. از آنجایی که حجم ثابت می ماند، کار انجام شده توسط سیستم صفر است. بنابراین سیستم کار نمی کند. اغلب اوقات، این ساده ترین متغیر ترمودینامیکی برای کنترل است. این فرآیند در یک ظرف مهر و موم شده رخ می دهد که نه منبسط می شود و نه منقبض می شود.

شکل 02: فرآیند ایزوکوریک
انرژی داخلی سیستم ترمودینامیکی با توجه به انتقال حرارت تغییر می کند. با این حال، تمام گرمای منتقل شده انرژی داخلی را افزایش یا کاهش می دهد. از آنجایی که ∆V صفر است، کار انجام شده توسط سیستم (یا کار انجام شده روی سیستم) نیز صفر است.اگر U انرژی داخلی و Q گرمای منتقل شده باشد؛
∆U=Q
تفاوت بین فرآیند ایزوباریک و ایزوکوریک چیست؟
فرایند ایزوباریک یک فرآیند شیمیایی است که در یک سیستم ترمودینامیکی تحت فشار ثابت انجام می شود در حالی که فرآیند ایزوکریک یک فرآیند شیمیایی است که در یک سیستم ترمودینامیکی تحت یک حجم ثابت انجام می شود. این تفاوت اصلی بین فرآیند ایزوباریک و ایزوکوریک است. این بدان معنی است که فشار سیستم ترمودینامیکی در طول یک فرآیند همسان بدون تغییر باقی میماند در حالی که فشار بر این اساس در یک فرآیند ایزوکوریک تغییر میکند. علاوه بر این، حجم سیستم ترمودینامیکی در طول یک فرآیند ایزوباریک تغییر می کند در حالی که حجم در طول یک فرآیند ایزوکوریک ثابت می ماند. با این حال، در هر دو فرآیند، انرژی داخلی سیستم تغییر می کند. اما بر خلاف فرآیند ایزوباریک، در طی یک فرآیند ایزوکوریک، تمام گرمایی که منتقل می شود یا به انرژی داخلی تبدیل می شود یا از انرژی داخلی می آید.
اینفوگرافیک زیر جزئیات بیشتری در مورد تفاوت بین فرآیند ایزوباریک و ایزوکوریک به شکل جدولی ارائه می دهد.

خلاصه - فرآیند ایزوباریک در مقابل فرآیند ایزوکوریک
هر دو فرآیند ایزوباریک و ایزوکوریک فرآیندهای ترمودینامیکی هستند که در سیستمهای ترمودینامیکی انجام میشوند و یک پارامتر را ثابت نگه میدارند. بنابراین، تفاوت بین فرآیند ایزوباریک و ایزوکوریک در این است که فرآیند ایزوباریک در فشار ثابت اتفاق میافتد در حالی که فرآیند ایزوباریک در حجم ثابت رخ میدهد.