تفاوت اصلی بین دهیدراتاسیون توسط H2SO4 و H3PO4 این است که کم آبی توسط H2SO4 ایمن تر است و واکنش پیچیده را تسهیل می کند، در حالی که آبگیری توسط H3PO4 ایمن تر است و واکنش پیچیده تر را تسهیل می کند.
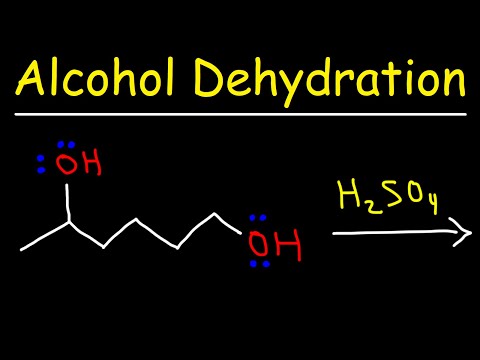
کم آبی اساساً حذف H2O است. آبگیری اتانول و سایر الکل ها را می توان با استفاده از دو کاتالیزور اسیدی مختلف انجام داد: اسید سولفوریک (H2SO4) و اسید فسفریک (V) (H3PO4). در این فرآیند، اتانول آبگیری می شود تا محصول آلکن بدست آید.
دهیدراتاسیون توسط H2SO4 چیست؟
آب زدایی توسط H2SO4 یک فرآیند شیمیایی است که در تشکیل آلکن ها از الکل ها با استفاده از اسید سولفوریک به عنوان کاتالیزور اسیدی مفید است.بنابراین، این واکنش شامل تشکیل یک ترکیب غیراشباع از یک ترکیب اشباع است. به عبارت دیگر، واکنش دهنده های این واکنش فقط دارای پیوند منفرد هستند، در حالی که محصولات این واکنش دارای پیوندهای منفرد و دوگانه هستند.
سولفوریک اسید یک کاتالیزور اسیدی برای کم آبی الکل ها است. در این فرآیند باید از اسید سولفوریک غلیظ استفاده کنیم. با این حال، استفاده از این کاتالیزور اسیدی نتایج تا حدودی کثیف می دهد. به این دلیل که اسید سولفوریک یک عامل اکسید کننده بسیار قوی است و می تواند برخی از الکل ها را کاهش دهد تا گاز دی اکسید کربن بدهد و خود را کاهش دهد تا گاز دی اکسید گوگرد تولید کند. بنابراین هر دو این گازها به عنوان آلاینده در محصول نهایی وجود دارند و باید حذف شوند. علاوه بر این، واکنش های دیگری نیز وجود دارد. به عنوان مثال، اسید سولفوریک با الکل واکنش می دهد و جرم کربن ایجاد می کند.

در فرآیند کم آبی، الکل با اسید سولفوریک در حالت غلیظ گرم می شود. در اینجا، مقدار اضافی اسید سولفوریک باید استفاده شود تا اطمینان حاصل شود که همه الکل ها با اسید واکنش می دهند. برای حذف گازهای ناخواسته تولید شده در این واکنش می توان از محلول هیدروکسید سدیم استفاده کرد.
دهیدراتاسیون توسط H3PO4 چیست؟
آب زدایی توسط H3PO4 یک فرآیند شیمیایی است که در تشکیل آلکن ها از الکل ها با استفاده از اسید فسفریک (V) به عنوان کاتالیزور اسیدی مفید است. بنابراین، این واکنش شامل تشکیل یک ترکیب غیراشباع از یک ترکیب اشباع است. به عبارت دیگر، واکنش دهنده های این واکنش فقط دارای پیوند منفرد هستند، در حالی که محصولات این واکنش دارای پیوندهای منفرد و دوگانه هستند.

شکل 02: واکنش کم آبی
مشابه روش فوق الذکر، این روش همچنین به کاتالیزور اسیدی در حالت غلیظ نیاز دارد. همچنین باید از مقدار زیادی اسید فسفریک (V) استفاده کنیم تا مطمئن شویم که تمام مولکول های الکل با کاتالیزور اسید واکنش داده و آلکن مورد نظر را به دست می آورند. علاوه بر این، کم آبی با استفاده از اسید فسفریک عمدتاً در تولید آلکن های حالت مایع استفاده می شود. مزیت اصلی این واکنش نسبت به آبگیری توسط اسید سولفوریک این است که این واکنش نتایج نامرتب به دست نمی دهد و نسبتاً بی خطر است (هیچ محصول مضری تولید نمی شود، به عنوان مثال دی اکسید گوگرد تولید می شود که از اسید سولفوریک به عنوان کاتالیزور اسیدی یک محصول مضر است).
تفاوت بین کم آبی توسط H2SO4 و H3PO4 چیست؟
آب زدایی توسط H2SO4 یک فرآیند شیمیایی است که در تشکیل آلکن ها از الکل ها با استفاده از اسید سولفوریک به عنوان کاتالیزور اسیدی مفید است. آبگیری توسط H3PO4 یک فرآیند شیمیایی است که در تشکیل آلکن ها از الکل ها با استفاده از اسید فسفریک (V) به عنوان کاتالیزور اسیدی مفید است.تفاوت اصلی بین دهیدراتاسیون توسط H2SO4 و H3PO4 در این است که کم آبی توسط H2SO4 ایمن تر است و یک واکنش پیچیده را تسهیل می کند، در حالی که کم آبی توسط H3PO4 ایمن تر است و واکنش پیچیده تر را تسهیل می کند.
در زیر اینفوگرافیک مقایسه های بیشتری را برای تشخیص تفاوت بین کم آبی توسط H2SO4 و H3PO4 نشان می دهد.

خلاصه - کم آبی توسط H2SO4 در مقابل H3PO4
آب زدایی اتانول و سایر الکل ها را می توان با استفاده از دو کاتالیزور اسیدی مختلف انجام داد. اسید سولفوریک و اسید فسفریک (V). تفاوت اصلی بین دهیدراتاسیون توسط H2SO4 و H3PO4 در این است که کم آبی توسط H2SO4 ایمن تر است و یک واکنش پیچیده را تسهیل می کند، در حالی که کم آبی توسط H3PO4 ایمن تر است و واکنش پیچیده تر را تسهیل می کند.
تقدیم به تصویر:
1. "Bogert-Cook Synthesis" توسط Mephisto spa - اثر شخصی (دامنه عمومی) از طریق Commons Wikimedia
2. «اتیلن تترا کربوکسیلیک دیانیدرید از طریق آبگیری اسیدی» نوشته DMacks (گفتگو) – کار شخصی (دامنه عمومی) از طریق ویکیمدیای مشترک