تفاوت کلیدی - Hyperconjugation در مقابل رزونانس
هایپرکونژوگه و رزونانس می توانند مولکول ها یا یون های چند اتمی را به دو روش مختلف تثبیت کنند. الزامات این دو فرآیند متفاوت است. اگر یک مولکول بتواند بیش از یک ساختار تشدید داشته باشد، آن مولکول دارای تثبیت رزونانس است. اما، هایپرکنژوگاسیون در حضور یک پیوند σ با یک اوربیتال p خالی یا نیمه پر یا یک اوربیتال π مجاور رخ می دهد. این تفاوت اصلی Hyperconjugation و Resonance است
Hyperconjugation چیست؟
برهمکنش الکترونها در یک پیوند σ (به طور کلی پیوندهای C-H یا C-C) با یک اوربیتال p خالی یا نیمه پر مجاور یا یک اوربیتال π منجر به یک اوربیتال مولکولی گسترده با افزایش پایداری سیستم می شود.این فعل و انفعال تثبیت کننده "هیپرکنژوگاسیون" نامیده می شود. بر اساس تئوری پیوند ظرفیت، این تعامل به عنوان "پیوند دوگانه بدون رزونانس پیوند" توصیف می شود.

Schreiner Hyperconjugation
رزونانس چیست؟
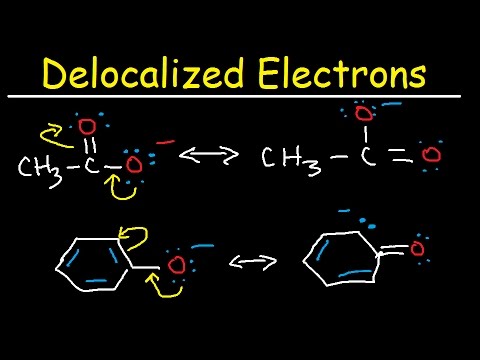
رزونانس روشی برای توصیف الکترونهای غیرمحلی در یک مولکول یا یون چند اتمی است که میتواند بیش از یک ساختار لوئیس برای بیان الگوی پیوند داشته باشد. چندین ساختار کمک کننده را می توان برای نشان دادن این الکترون های غیرمحلی در یک مولکول یا یک یون استفاده کرد و این ساختارها ساختارهای تشدید نامیده می شوند. تمام ساختارهای کمک کننده را می توان با استفاده از ساختار لوئیس با تعداد قابل شمارش پیوند کووالانسی با توزیع جفت الکترون بین دو اتم در پیوند نشان داد.از آنجایی که می توان از چندین ساختار لوئیس برای نشان دادن ساختار مولکولی استفاده کرد. ساختار مولکولی واقعی یک واسطه از تمام آن ساختارهای ممکن لوئیس است. هیبرید رزونانسی نامیده می شود. همه ساختارهای کمک کننده هسته ها را در یک موقعیت دارند، اما توزیع الکترون ها می تواند متفاوت باشد.

رزونانس فنل
تفاوت بین Hyperconjugation و Resonance چیست؟
ویژگی هایپرکونژوگه و رزونانس
Hyperconjugation
Hyperconjugation بر طول پیوند تأثیر می گذارد و منجر به کوتاه شدن پیوندهای سیگما (پیوندهای σ) می شود
| مولکول | طول پیوند C-C | دلیل |
| 1، 3-Butadiene | 1.46 A | کونژوگاسیون طبیعی بین دو بخش آلکنیل. |
| متیل استیلن | 1.46 A | Hyperconjugation بین قسمت های آلکیل و آلکینیل |
| متان | 1.54 A | این یک هیدروکربن اشباع است بدون اضافه کنژوگه |
مولکول های دارای بیش کونژوگیگاسیون در مقایسه با مجموع انرژی های پیوندشان مقادیر بیشتری برای گرمای تشکیل دارند. اما، گرمای هیدروژناسیون در هر پیوند دوگانه کمتر از گرمای اتیلن است
پایداری کربوکاتیون ها بسته به تعداد پیوندهای C-H متصل به اتم کربن با بار مثبت متفاوت است. هنگامی که بسیاری از پیوندهای C-H متصل می شوند، تثبیت هایپرکنژوگاسیون بیشتر است
(CH3)3C+ > (CH3)2CH+ > (CH3)CH 2+ > CH3+
قدرت هایپرکنژوگاسیون نسبی به نوع ایزوتوپ هیدروژن بستگی دارد. هیدروژن در مقایسه با دوتریوم (D) و تریتیوم (T) استحکام بیشتری دارد. تریتیوم در بین آنها کمترین توانایی را برای نشان دادن هایپرکونژوگه دارد. انرژی مورد نیاز برای شکستن پیوند C-T > پیوند C-D > پیوند C-H، و این باعث میشود H به بیشهمنژوگاسیون راحتتر شود
رزونانس